I. Grundlagen der Blutgruppenserologie
Eine Transfusion bezeichnet die Übertragung von Blut oder einzelnen Blutbestandteilen von einem Spender auf einen Empfänger. Sie stellt eine wichtige therapeutische Maßnahme dar und wird eingesetzt, um fehlende oder gestörte Funktionen des Blutes gezielt zu ersetzen.
Ziel einer Transfusion ist es, entweder fehlende Blutzellen zu substituieren, Gerinnungsfaktoren zu ergänzen oder ein vermindertes Blutvolumen auszugleichen.
Während früher häufig Vollblut transfundiert wurde, erfolgt heute nahezu ausschließlich eine Komponententherapie. Dabei erhält der Patient nur die Blutbestandteile, die er tatsächlich benötigt. Dies erhöht die Wirksamkeit und reduziert gleichzeitig das Risiko von Nebenwirkungen.
a) Wichtige Blutprodukte
Erythrozytenkonzentrate (EK)
Erythrozytenkonzentrate enthalten vor allem rote Blutkörperchen und werden eingesetzt, um die Sauerstofftransportkapazität des Blutes zu verbessern.
Typische Indikationen sind schwere Anämien, akuter Blutverlust sowie symptomatische Patienten, beispielsweise mit Dyspnoe oder Schwindel.
Als grober Richtwert gilt ein Hämoglobinwert unter etwa 7–8 g/dl, wobei stets die klinische Situation des Patienten entscheidend ist.


Thrombozytenkonzentrate (TK)
Thrombozytenkonzentrate enthalten Blutplättchen und dienen der Stabilisierung der primären Hämostase.
Sie werden eingesetzt bei Thrombozytopenie, erhöhter Blutungsgefahr sowie bei aktiven Blutungen.
Typische Richtwerte sind eine Thrombozytenzahl unter 10.000/µl für eine prophylaktische Gabe sowie unter 50.000/µl vor operativen Eingriffen.
Frischplasma (Fresh Frozen Plasma, FFP)
Frischplasma enthält eine Vielzahl an Gerinnungsfaktoren und wird eingesetzt, um Störungen der sekundären Hämostase auszugleichen.
Typische Indikationen sind Gerinnungsstörungen, massive Blutungen sowie die disseminierte intravasale Gerinnung (DIC).

b) Risiken der Transfusion
Trotz moderner Sicherheitsstandards ist eine Transfusion immer mit Risiken verbunden. Zu den wichtigsten zählen immunologische Reaktionen, die Übertragung von Infektionen, die heute jedoch selten ist, sowie eine mögliche Volumenüberladung des Kreislaufs.
Aus diesem Grund sollten Transfusionen nur durchgeführt werden, wenn sie medizinisch notwendig sind.
c) Voraussetzungen für Transfusionen
Vor jeder Transfusion müssen bestimmte Voraussetzungen erfüllt sein, um die Sicherheit des Patienten zu gewährleisten.
Dazu gehören die Bestimmung der Blutgruppe, die Prüfung der Verträglichkeit, beispielsweise durch eine Kreuzprobe, sowie die eindeutige Identifikation des Patienten.
Diese Maßnahmen sind entscheidend, um schwerwiegende Komplikationen, insbesondere hämolytische Transfusionsreaktionen, zu vermeiden.
II. Blutgruppensysteme
Blutgruppensysteme beruhen auf dem Vorhandensein spezifischer Antigene auf der Oberfläche von Erythrozyten sowie den dazugehörigen Antikörpern im Plasma. Treffen passende Antigene und Antikörper aufeinander, kann es zu einer Immunreaktion kommen.
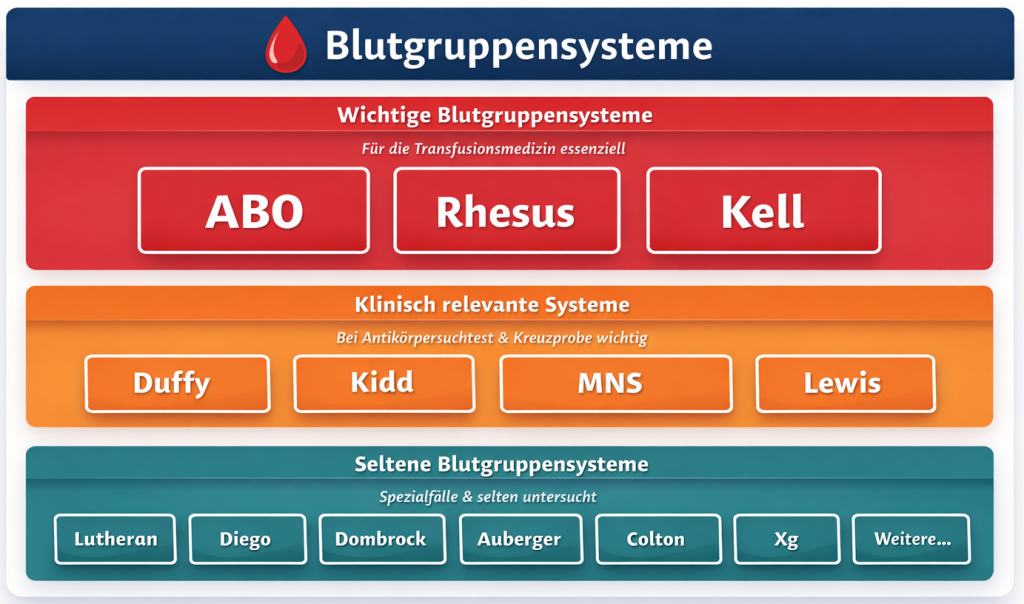
Insgesamt sind etwa 30 Blutgruppensysteme bekannt. Die wichtigsten für die klinische Praxis sind das AB0-System, das Rhesus-System und das Kell-System. Weitere Systeme sind beispielsweise Diego, Lewis, Duffy, Kidd, Lutheran, Auberger und Dombrock (siehe Abbildung 4).
Damit lassen sich sich mehr als 600 verschiedene Blutgruppen definieren. Am bedeutendsten sind die Merkmale des AB0- und Rhesus-Systems. Diese werden bereits in der 6. Schwangerschaftswoche vom Embryo ausgebildet.
Blutgrupppenantigene
Die Antigene des AB0-Systems sind Oligosaccharide oder Polypeptide, die an Membranlipiden gebunden sind oder über über hydrophobe Anteile der Biomembran integriert sind.
Die Antigene des Rhesususystems sind Proteinantigene, d.h. das Blutgruppenepitop ist Bestandteil eines Proteins und keines Kohlenhydrats. Sie sind auch am Aufbau des Membranskeletts der Erythrozytenmebran beteiligt und sind daher dort eingebettet.
a) AB0-System
Das AB0-System wurde im Jahr 1900 von Karl Landsteiner entdeckt und stellt das wichtigste Blutgruppensystem in der Transfusionsmedizin dar. Die AB0-Antigene finden wir zudem nahezu auf allen Körperzellen.
Aufbau
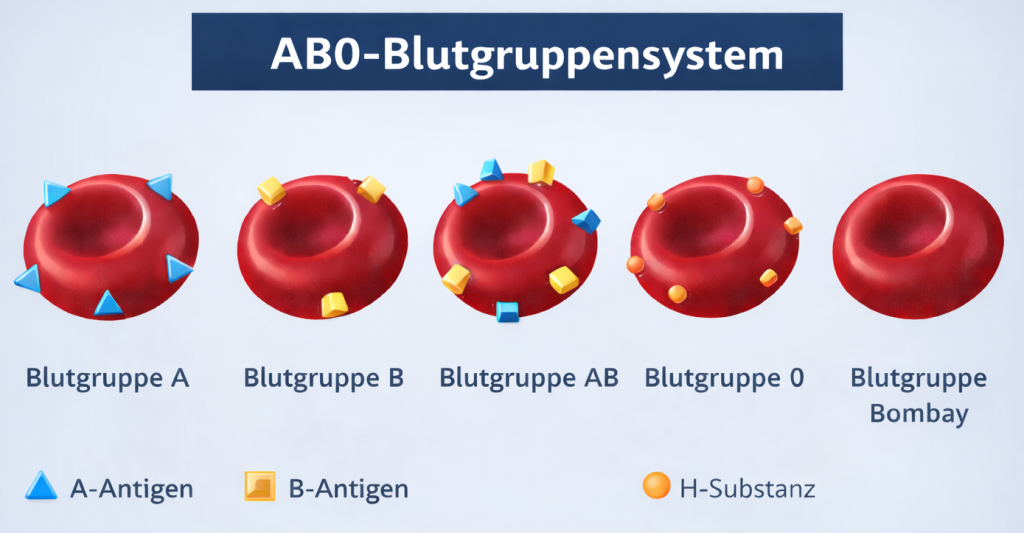
Das AB0-Blutgruppensystem basiert auf drei zentralen Antigenstrukturen: dem A-Antigen, dem B-Antigen und der sogenannten H-Substanz. Die genetische Grundlage hierfür liegt auf Chromosom 9, wobei jeder Mensch zwei Allele besitzt – jeweils eines von jedem Elternteil.
Diese Allele codieren für Enzyme, sogenannte Glykosyltransferasen, die an die H-Substanz auf der Oberfläche der Erythrozyten anbauen. Das A-Allel führt zur Bindung der A-Substanz an die H-Substanz und daraus resultiert das A-Antigen. Entsprechend bewirkt das B-Allel die Bindung der B-Substanz an die H-Substanz. Das 0-Allel hingegen codiert für kein funktionsfähiges Enzym, sodass die H-Substanz unverändert bestehen bleibt.
Daraus ergeben sich die verschiedenen Blutgruppen: Bei Blutgruppe A werden A-Antigene gebildet, bei Blutgruppe B B-Antigene und bei Blutgruppe AB beide Strukturen gleichzeitig.
Eine Besonderheit stellt die Bombay-Blutgruppe dar, bei der die H-Substanz selbst fehlt, sodass weder A- noch B-Antigene entstehen können. Der Genotyp von Bombay wird daher als „hh“ beschrieben (siehe Abbildung 5).
Sonderfall: Bombay-Phänotyp (Wahrscheinlichkeit 1/300.000)
Beim Bombay-Phänotyp dürfen Patienten nur den Bombay-Phänotyp transfundiert bekommen. Blutgruppe 0 Rhesus negativ entfällt als Universalspender hier.
Vererbung
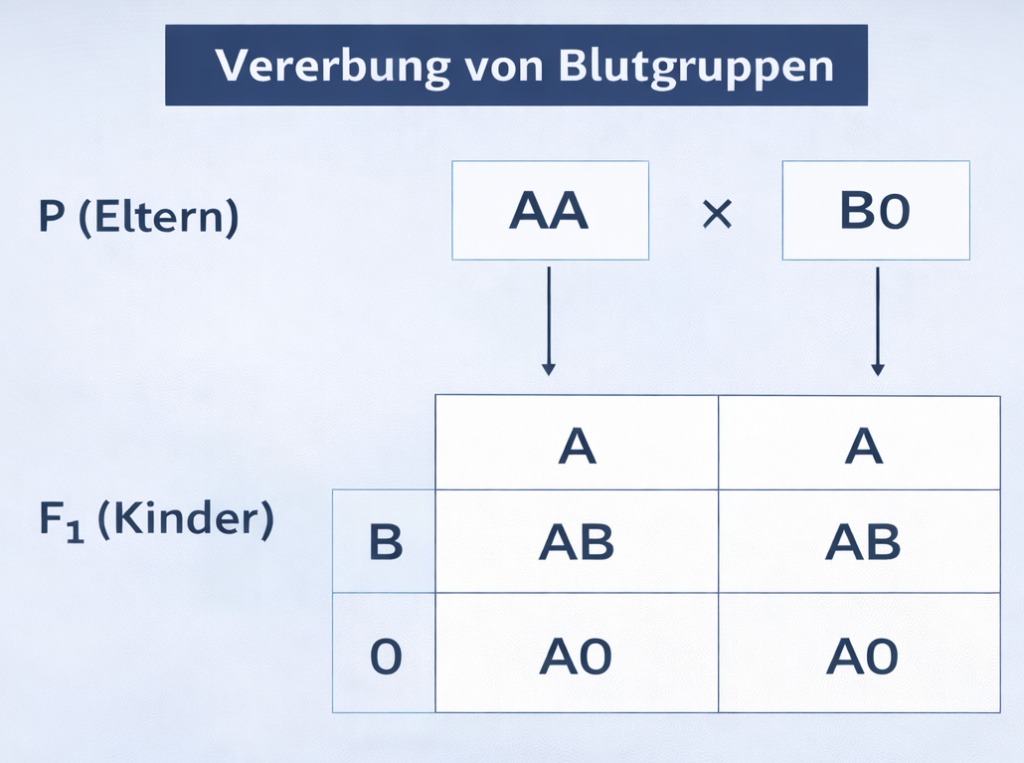
Die Vererbung der Blutgruppen im AB0-System basiert auf der Weitergabe von drei möglichen Allelen: A, B und 0 (Null). Jeder Mensch besitzt zwei Allele, jeweils eines von jedem Elternteil. Dabei sind die Allele A und B codominant, während das Allel 0 rezessiv ist. Das bedeutet, dass A und B gemeinsam ausgeprägt werden können, während 0 nur sichtbar wird, wenn es doppelt vorliegt.
Im vorliegenden Beispiel wird ein Elternteil mit dem Genotyp AA mit einem Elternteil mit dem Genotyp B0 kombiniert. Das erste Elternteil kann ausschließlich das Allel A weitergeben, während das zweite Elternteil entweder B oder 0 vererben kann. Bei der Befruchtung erhält das Kind jeweils ein Allel von beiden Elternteilen.
Daraus ergeben sich zwei mögliche Genotypen: AB und A0. Diese treten jeweils mit einer Wahrscheinlichkeit von 50 % auf. Kinder mit dem Genotyp AB haben die Blutgruppe AB, da beide Allele gleichwertig ausgeprägt werden. Kinder mit dem Genotyp A0 zeigen die Blutgruppe A, da das dominante Allel A das rezessive Allel 0 überdeckt.
Eine Blutgruppe 0 ist in diesem Fall nicht möglich, da hierfür zwei 0-Allele erforderlich wären!
Untergruppen
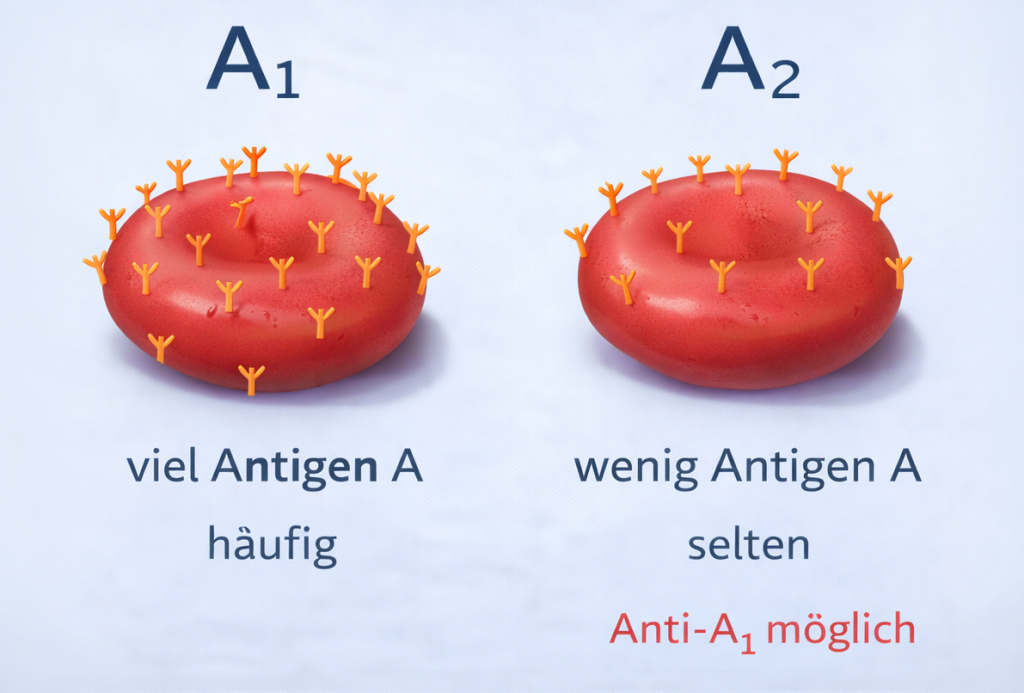
Innerhalb des AB0-Systems existieren Untergruppen der Blutgruppe A, insbesondere A1 und A2. Diese unterscheiden sich nicht in der Art des Antigens, sondern in der Menge der A-Antigene auf der Oberfläche der Erythrozyten (siehe ABbildung 7).
Bei der Untergruppe A1 sind viele A-Antigene auf der Zelloberfläche vorhanden, weshalb sie in der Blutgruppenbestimmung in der Regel eine starke Reaktion zeigt und zudem die häufigste Form darstellt. Im Gegensatz dazu trägt die Untergruppe A2 deutlich weniger A-Antigene. Dadurch kann die Reaktion in serologischen Tests schwächer ausfallen.
Diese geringere Antigenmenge hat auch klinische Bedeutung: Bei Personen mit Blutgruppe A2 kann es zur Bildung von Anti-A1-Antikörpern kommen. Insgesamt kann eine unerwartet schwache Reaktion in der Blutgruppenbestimmung daher auf das Vorliegen einer solchen Untergruppe hinweisen.
Häufigkeiten
Die Verteilung der Blutgruppen in der Bevölkerung ist unterschiedlich:
- Blutgruppe A: etwa 44 %
- Blutgruppe 0: etwa 42 %
- Blutgruppe B: etwa 10 %
- Blutgruppe AB: etwa 4 %
Antikörper
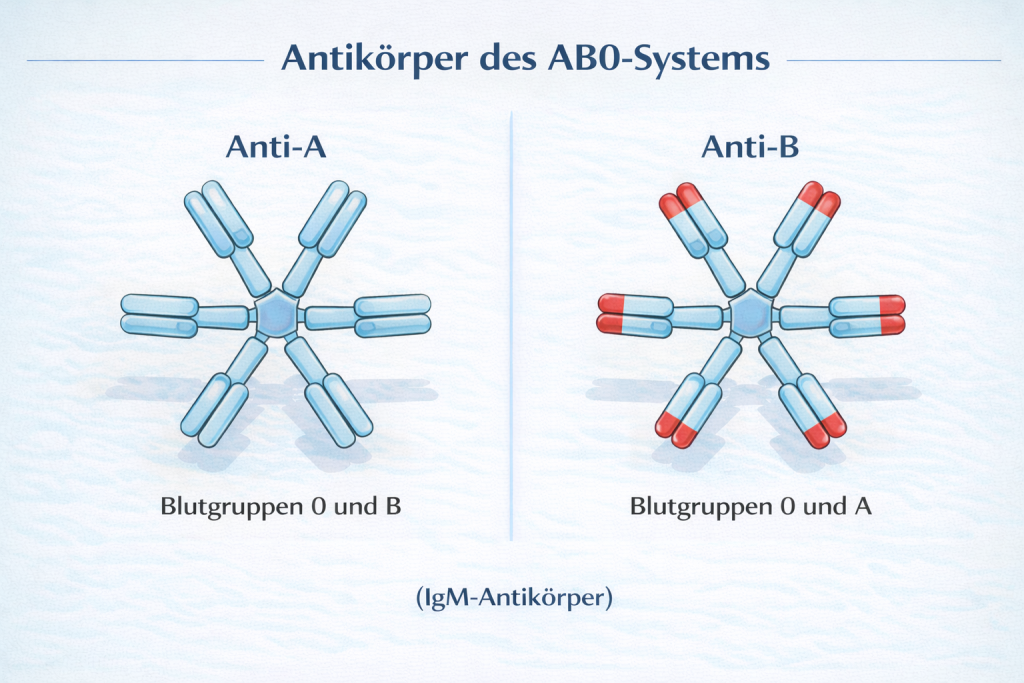
Im AB0-System kommen sogenannte natürliche Antikörper (Alloantikörper) vor, die vom Typ IgM sind und nicht plazentagängig sind. Sie entstehen erst nach der Geburt, meist zwischen dem dritten und sechsten Lebensmonat. Auslöser ist die Ähnlichkeit von Antigenstrukturen auf Darmbakterien mit den AB0-Antigenen, wodurch das Immunsystem zur Antikörperbildung angeregt wird.
Dabei existieren zwei wichtige Antikörper: Anti-A, der gegen das A-Antigen gerichtet ist, und Anti-B, der gegen das B-Antigen wirkt. Welche Antikörper im Blut vorhanden sind, hängt direkt von der eigenen Blutgruppe ab.
Nach der Landsteiner-Regel bildet ein Mensch immer Antikörper gegen die Antigene, die er selbst nicht auf seinen Erythrozyten trägt. Daher besitzt eine Person mit Blutgruppe A Anti-B-Antikörper, eine Person mit Blutgruppe B Anti-A-Antikörper, während Personen mit Blutgruppe AB keine dieser Antikörper haben. Menschen mit Blutgruppe 0 bilden hingegen sowohl Anti-A- als auch Anti-B-Antikörper (siehe Abbilung 8).
b) Rhesus-System
Das Rhesus-System wurde ebenfalls von Karl Landsteiner um 1940 entdeckt und stellt nach dem AB0-System das zweitwichtigste Blutgruppensystem dar. Kein anderes Blutgruppensystem weist eine so hohe Antigenvielfalt auf. Man kennt heute mehr als 50 Varainten.
Aufbau und Vererbung
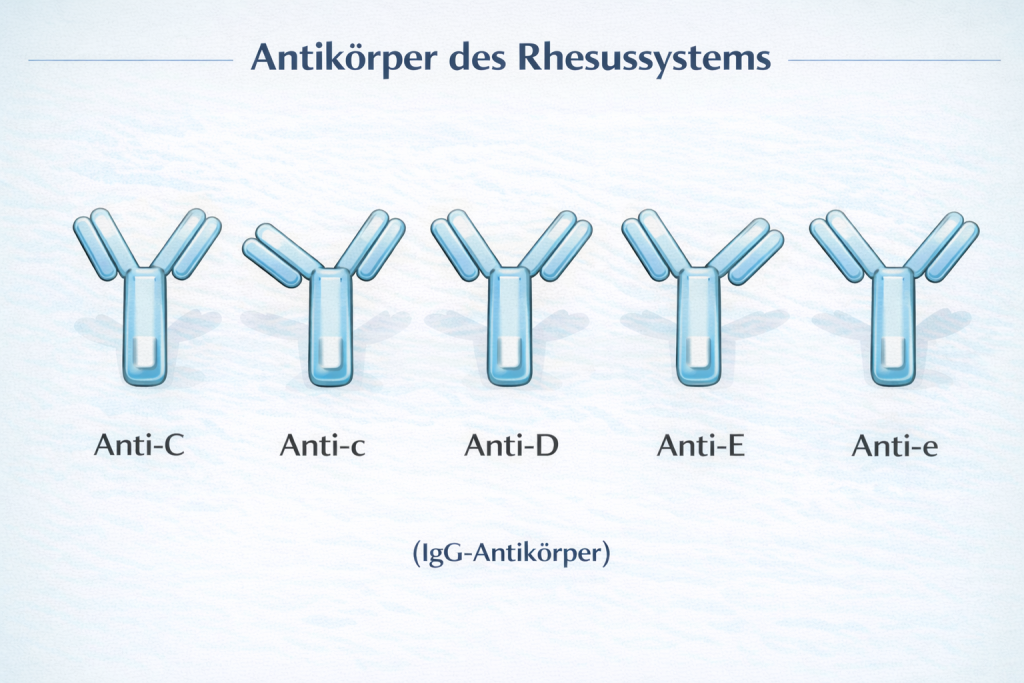
Das System umfasst fünf Hauptantigene: C, c, D, E und e. Diese befinden sich ausschließlich auf den Erythrozyten.
Das sogenannte „d“ stellt kein echtes Antigen dar, sondern beschreibt das Fehlen des D-Antigens.
Der umgangssprachliche „Rhesusfaktor“ entspricht dem Antigen D. Dieses besitzt die höchste Antigenität innerhalb des Rhesus-Systems und ist daher klinisch besonders relevant.

Die genetischen Informationen sind auf Chromosom 1 codiert. Auch hier erfolgt die Vererbung codominant.
Rhesusformel
Die Rhesusformel beschreibt, welche Antigene auf den Erythrozyten vorhanden sind. Sie besteht aus sechs Positionen, beispielsweise:
- CcDDEe: alle genannten Antigene sind vorhanden
- ccddee: nur die Antigene c und e sind vorhanden
Für die Antigene C/c und E/e ergeben sich jeweils drei mögliche Kombinationen. Am Beispiel von Antigen C und c: CC, cc oder Cc (homozygot oder heterozygot). Für das Antigen D wird in der Praxis meist nur zwischen vorhanden (D.) und nicht vorhanden (dd) unterschieden. „D.“ entspricht hierbei den Kombinationen DD oder Dd. Hier ist eine konkrete Aufschlüsselung nicht relevant, da das Vorhandensein eines D-Antigen immer Rhesus-positiv bedeutet.
Varianten des Rhesus-D-Antigens
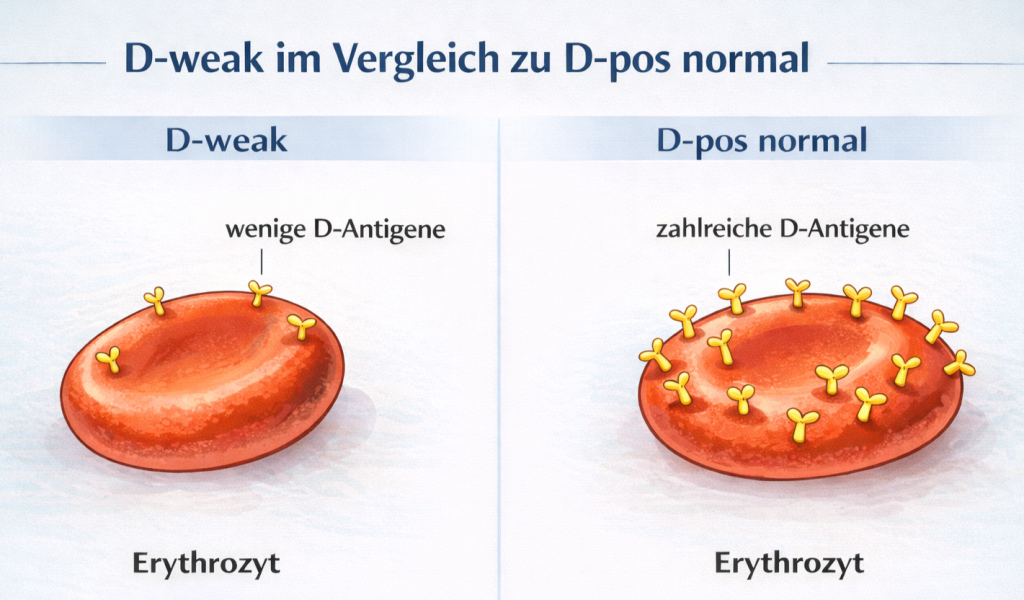
D-weak
Bei dieser Variante ist das D-Antigen nur schwach ausgeprägt. Betroffene Personen besitzen eine geringe Anzahl an D-Antigenen auf ihren Erythrozyten. In seltenen Fällen können Antikörper gebildet werden. In der Praxis werden diese Personen meist als Rhesus-positiv eingestuft, wobei im Transfusionskontext besondere Vorsicht erforderlich ist.
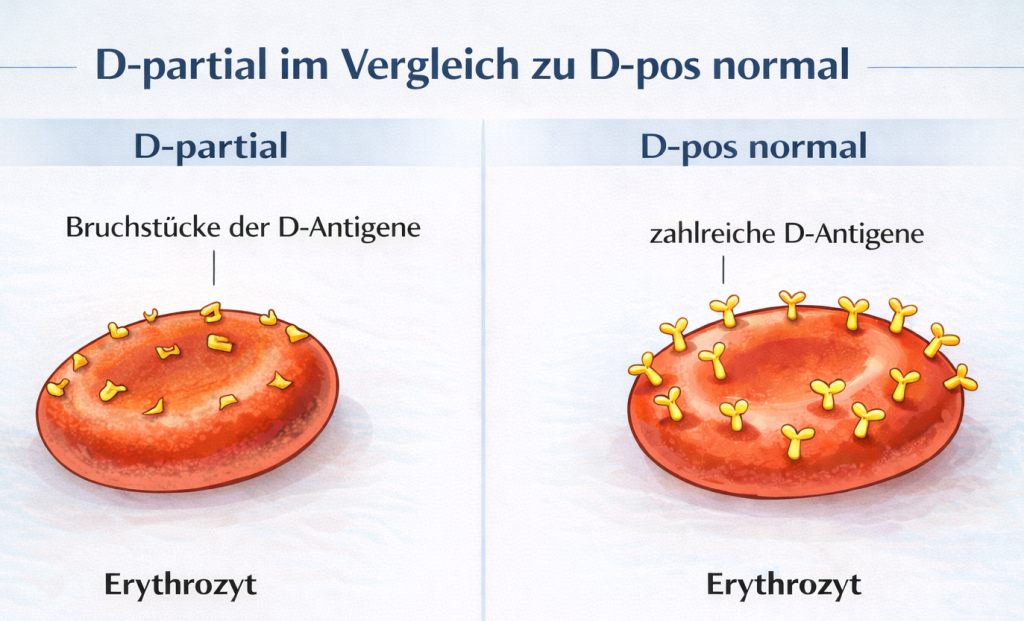
D-partial
Hier liegt ein unvollständig ausgebildetes D-Antigen vor, bei dem bestimmte Bausteine („Epitope“) fehlen. Gegen diese fehlenden Strukturen können bei Kontakt mit vollständigem D-Antigen Antikörper gebildet werden. Labordiagnostisch erscheinen diese Patienten häufig als Rhesus-positiv, können jedoch im indirekten Coombs-Test Rhesus-Antikörper nachweisen und somit ein Risiko für Transfusionsreaktionen darstellen.
Antikörper
Im Gegensatz zum AB0-System existieren im Rhesus-System keine natürlichen Antikörper. Diese entstehen erst nach Kontakt mit fremdem Blut, beispielsweise durch Transfusion oder Schwangerschaft.
Rhesus-Antikörper sind meist vom Typ IgG (siehe Abbildung 12), plazentagängig und können nicht allein eine sichtbare Agglutination auslösen. Sie werden daher als inkomplette Antikörper bezeichnet.
III. Problemfall MHN - morbus haemolyticus neonatorum
Entstehung
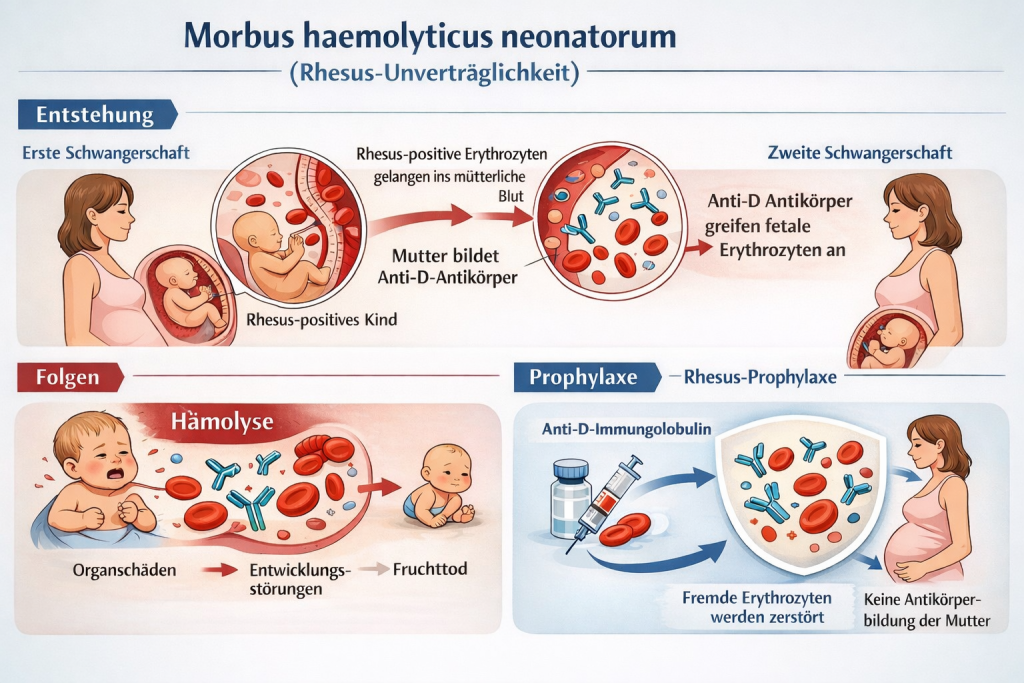
Eine rhesusnegative Mutter bekam zuerst ein rhesuspositives Kind. Im Verlauf der Geburt passieren kindliche Erythrozyten in den mütterlichen Kreislauf. Das Immunsystem der Mutter erkennt das D-Antigen auf diesen fremden Erythrozyten als körperfremd und wird daraufhin aktiviert. In der Folge kommt es zur Bildung spezifischer Antikörper gegen das D-Antigen. Bei einer erneuten Schwangerschaft mit einem Rhesus-positiven Kind können diese Antikörper die Plazenta passieren und zur Zerstörung fetaler Erythrozyten führen.
Folgen
Die resultierende Hämolyse kann zu schweren Organschäden, Entwicklungsstörungen oder im schlimmsten Fall zum intrauterinen Fruchttod führen.
Prophylaxe
Zur Vermeidung dieser Immunisierung wird eine Rhesus-Prophylaxe durchgeführt. Dabei erhält die Mutter Anti-D-Immunglobulin (Antikörper gegen Rhesus-D) während der Schwangerschaft sowie nach der Geburt gespritzt.
Diese Antikörper eliminieren fetale Erythrozyten im mütterlichen Blutkreislauf, bevor das Immunsystem der Mutter aktiviert wird. Die Mutter bildet somit keinen eigenen Antikörper gegen Rhesus D.
IV. Blutgruppenbestimmung
Die Blutgruppenbestimmung basiert auf einer Antigen-Antikörper-Reaktion, bei der es entweder zu einer Agglutination (positiv) oder zu keiner Reaktion (negativ) kommt. Voraussetzung ist zunächst die Auftrennung des Blutes durch Zentrifugation in Plasma und Blutzellen. Das Plasma wird anschließend in ein separates Röhrchen überführt. Aus dem verbleibenden Blutkuchen werden Erythrozyten entnommen (ca. 25 µl) und mit 500 µl 0,9 % NaCl zu einer Suspension vermischt. Diese sollte eine kirschrote, eher kräftige Färbung aufweisen.
Untersucht werden dabei mehrere Komponenten: Zum einen die A- und B-Antigene auf den Erythrozyten zur Bestimmung der AB0-Blutgruppe sowie die Rhesus-Antigene für die Bestimmung des Rhesusfaktors. Zusätzlich erfolgt eine Serumgegenprobe zum Nachweis der natürlichen Antikörper des AB0-Systems und ein Antikörpersuchtest zum Nachweis irregulärer Antikörper, beispielsweise gegen Rhesus-Antigene.

Die Testung erfolgt häufig im Gelkartenprinzip, beispielsweise nach BIORAD. Für die Bestimmung von AB0- und Rhesusmerkmalen werden etwa 12,5 µl der Erythrozytensuspension in die entsprechenden Gelkarten („DiaClon AB0+DAT“, sowie „Rh-Subgroups + K (mono & pheno)“ pipettiert und anschließend bei etwa 900 U/min für 10 Minuten zentrifugiert. Für die Serumgegenprobe werden die Testzellen aus dem DiaCell-Reagenz AB0 verwendet, welche definierte AB0-Antigenen aufweisen und in die Gelkarte „NaCl, Enyzme Test [..]“ gegeben. Dann werden diese mit etwa 50 µl Patientenplasma versetzt. Nach einer kurzen Inkubation von 10 min bei Raumtemperatur folgt ebenfalls die Zentrifugation. Beim Antikörpersuchtest werden Suchzellen mit bekannten Antigenmustern eingesetzt (DiaCell-Reagenz-I,II,III). Diese werden in die passende Gelkarte „LISS/Coombs“ gegeben und mit 25 μl Patientenplasma inkubiert. Typischerweise 15 Minuten bei 37 °C, um die Reaktion unter körpernahen Bedingungen zu ermöglichen, bevor auch hier zentrifugiert wird.
Die Auswertung erfolgt im Vier-Augen-Prinzip. Eine positive Reaktion zeigt sich durch Agglutination: Die Erythrozyten bleiben als rote Bande in oder auf der Gelschicht liegen. Bei einer negativen Reaktion sinken die Erythrozyten vollständig auf den Boden der Vertiefung ab. Je nach Stärke der Agglutination können unterschiedliche Grade beobachtet werden, die von schwachen „Wölkchen“ bis hin zu starken Reaktionen reichen und in Stufen von „+“ bis „++++ “ eingeteilt werden können.

V. Verträglichkeit von Bluttransfusionen
=> eine Transfusion ist möglich, wenn keine Antigen-Antikörper-Reaktion stattfindet, sobald Spender- und Empfängerblut aufeinander treffen
a) AB0-Kompatibilität
Die AB0-Kompatibilität stellt die wichtigste Voraussetzung für eine sichere Bluttransfusion dar. Bereits geringe Mengen inkompatiblen Blutes können zu schweren immunologischen Reaktionen führen.
Grundlage der Verträglichkeit ist das Zusammenspiel von Antigenen auf den Erythrozyten des Spenders und den Antikörpern im Plasma des Empfängers. Eine Transfusion ist nur dann sicher, wenn die Antigene des Spenders nicht von den Antikörpern des Empfängers erkannt werden.
Kommt es zu einer Inkompatibilität, binden die Antikörper des Empfängers an die Erythrozyten des Spenders. Dies führt zur Agglutination und in der Folge zur Hämolyse der transfundierten Zellen.
Die Verträglichkeit bei der Transfusion von Erythrozytenkonzentraten ergibt sich aus den Eigenschaften der jeweiligen Blutgruppen:
- Blutgruppe 0 besitzt keine Antigene auf den Erythrozyten und kann daher grundsätzlich allen Blutgruppen Erythrozyten spenden
- Blutgruppe A trägt Antigen A und kann an Patienten mit Blutgruppe A oder AB spenden
- Blutgruppe B trägt Antigen B und kann an Patienten mit Blutgruppe B oder AB spenden
- Blutgruppe AB trägt sowohl Antigen A als auch B und kann nur an Patienten mit Blutgruppe AB spenden
=> Daraus ergibt sich, dass Blutgruppe 0 als Universalspender für Erythrozyten gilt, während Blutgruppe AB als Universalempfänger bezeichnet wird.
Zu beachten ist, dass sich diese Regeln auf die Transfusion von Erythrozytenkonzentraten beziehen. Bei der Gabe von Plasma gelten umgekehrte Verhältnisse, da hier die Antikörper des Spenders eine entscheidende Rolle spielen.
Trotz bekannter Blutgruppe wird vor jeder Transfusion eine Verträglichkeitsprüfung durchgeführt, da neben dem AB0-System auch weitere Blutgruppensysteme eine Rolle spielen können.
Eine Missachtung der AB0-Kompatibilität kann zu einer akuten hämolytischen Transfusionsreaktion führen, die durch Fieber, Schock und Organversagen gekennzeichnet ist und eine lebensbedrohliche Situation darstellt.
b) Rhesus-Kompatibilität
In der Transfusionsmedizin wird grundsätzlich angestrebt, möglichst rhesuskompatibel zu transfundieren. Das bedeutet, dass die Rhesusformel von Spender und Empfänger übereinstimmt beziehungsweise keine relevanten Antigenunterschiede vorliegen.
Ist keine vollständige Rhesuskompatibilität gegeben, besteht die Gefahr, dass der Empfänger Antikörper gegen fremde Rhesus-Antigene bildet. Diese Immunisierung ist insbesondere für zukünftige Transfusionen oder Schwangerschaften von Bedeutung.
Ein praktisches Problem besteht darin, dass vollständig rhesuskompatible Blutkonserven nicht immer verfügbar sind. In bestimmten Situationen kann daher eine rhesusinkompatible Transfusion notwendig werden.
Bei Frauen im gebärfähigen Alter sowie bei Mädchen wird eine rhesusinkompatible Transfusion nur im absoluten Notfall durchgeführt, beispielsweise bei lebensbedrohlichem Blutverlust. Hintergrund ist das Risiko eines Morbus haemolyticus neonatorum bei späteren Schwangerschaften.
Hat ein rhesusnegativer Patient rhesuspositives Blut erhalten, sollte nach etwa zwei bis vier Monaten eine Kontrolle auf die Bildung von Rhesus-Antikörpern erfolgen.
Mögliche Konsequenzen einer Immunisierung sind:
- Bildung von Antikörpern gegen Rhesus-Antigene
- erschwerte Bereitstellung kompatibler Blutkonserven bei zukünftigen Transfusionen
- Risiko für Schwangerschaftskomplikationen
Werden Antikörper nachgewiesen, erhält der Patient in der Regel einen entsprechenden Hinweis, beispielsweise in Form eines Notfallausweises, der auf die bestehende Immunisierung aufmerksam macht.
Diese Problematik ist nicht nur bei Erythrozytenkonzentraten relevant, sondern kann auch bei der Gabe von Thrombozytenkonzentraten auftreten.
VI. Antikörpersuchtest
Neben den bekannten Blutgruppensystemen wie AB0 und Rhesus existieren zahlreiche weitere Blutgruppenantigene. Diese können ebenfalls immunologisch relevant sein. Ein Patient kann Antikörper gegen solche seltenen Antigene besitzen, sodass es trotz scheinbar passender Blutgruppe zu einer Unverträglichkeit kommen kann. Der Antikörpersuchtest dient dem Nachweis sogenannter irregulärer Antikörper im Plasma des Patienten. Diese Antikörper richten sich gegen Blutgruppenantigene, die nicht zum AB0-System gehören.
Prinzip
Beim Antikörpersuchtest wird das Plasma des Patienten mit Testerythrozyten, sogenannten Suchzellen, zusammengebracht. Kommt es zur Agglutination, weist dies auf das Vorhandensein von Antikörpern hin.
a) Indirekter Coombs-Test
Der indirekte Coombs-Test dient dem Nachweis freier Antikörper im Plasma.
Er wird durchgeführt:
- begleitend zur Blutgruppenbestimmung und vor jeder Transfusion
- bei auffälliger Eigenkontrolle
- im Rahmen der Schwangerschaftsvorsorge
Durchführung
Das Plasma des Patienten wird mit Suchzellen inkubiert. Diese Suchzellen sind Erythrozyten mit definierter Antigenstruktur. Da verschiedene Suchzellen unterschiedliche Antigene tragen, kann eine breite Palette möglicher Antikörper erfasst werden.
Sind irreguläre Antikörper vorhanden, binden diese an die Antigene der Suchzellen. Da es sich häufig um inkomplette Antikörper handelt, wird Antihumanglobulin (AHG) mit ins Reagenz zugegeben, um die gebundenen Antikörper sichtbar zu machen. Führt dies zur Agglutination, ist der Test positiv.

b) Direkter Coombs-Test
Der direkte Coombs-Test dient dem Nachweis von Antikörpern, die bereits an Erythrozyten gebunden sind.
Hierbei wird Antihumanglobulin zu den Erythrozyten gegeben. Dieses bindet an die schweren Ketten der gebundenen Antikörper und führt zur Agglutination. Der Test ist insbesondere bei der Abklärung von Hämolysen von Bedeutung.

VII. Kreuzprobe
Die Kreuzprobe stellt den finalen Sicherheitscheck vor jeder Transfusion dar. Sie überprüft direkt die Verträglichkeit zwischen Spender und Empfänger.
Prinzip
Bei der Kreuzprobe wird das Plasma des Patienten mit den Erythrozyten des vorgesehenen Spenders zusammengebracht.
- Keine Agglutination bedeutet, dass die Transfusion als kompatibel gilt
- Eine Agglutination zeigt eine Inkompatibilität an und stellt eine Kontraindikation für die Transfusion dar
Die Kreuzprobe berücksichtigt nicht nur das AB0- und Rhesus-System, sondern auch weitere, möglicherweise klinisch relevante Antigene. Sie dient somit als praktische Simulation der Transfusion im Labor.
Durchführung in der Praxis
Vor einer Transfusion erfolgt in der Regel:
- Bestimmung der Blutgruppe
- Durchführung eines Antikörpersuchtests
- anschließende Kreuzprobe mit der ausgewählten Blutkonserve
Erst wenn alle Untersuchungen unauffällig sind, wird die Transfusion freigegeben.
Kreuzprobe – Gelkartenprinzip nach BIORAD
Es werden zunächst etwa 10 µl Erythrozyten aus dem Segment des Erythrozytenkonzentrats in 1000 µl 0,9 % NaCl überführt und sorgfältig vermischt, um eine homogene Suspension herzustellen.
Anschließend werden 50 µl dieser Erythrozytensuspension in eine LISS/Coombs-Gelkarte pipettiert und mit 25 µl Patientenplasma versetzt. Die Mischung wird für etwa 15 Minuten bei 37 °C inkubiert, um eine mögliche Antigen-Antikörper-Reaktion unter körpernahen Bedingungen zu ermöglichen. Danach erfolgt die Zentrifugation bei etwa 900 U/min für 10 Minuten.
Die Auswertung erfolgt im Vier-Augen-Prinzip. Eine Agglutination zeigt eine Unverträglichkeit an, während ein negatives Ergebnis bedeutet, dass die Erythrozyten des Spenders mit dem Plasma des Empfängers kompatibel sind.
=> Die Kreuzprobe ist damit ein entscheidender Bestandteil der Transfusionssicherheit und trägt maßgeblich dazu bei, hämolytische Transfusionsreaktionen zu verhindern!

VIII. Transfusionsreaktionen
Transfusionsreaktionen sind unerwünschte Reaktionen, die im zeitlichen Zusammenhang mit einer Bluttransfusion auftreten. Sie entstehen in der Regel durch Unverträglichkeiten zwischen Spender und Empfänger oder durch immunologische Reaktionen auf transfundierte Blutbestandteile.
Prinzip
Transfusionsreaktionen entstehen durch:
- immunologische Reaktionen gegen fremde Antigene
- Unverträglichkeiten zwischen Spender- und Empfängerblut
a) Akute hämolytische Transfusionsreaktionen
Die akute hämolytische Transfusionsreaktion stellt die schwerwiegendste Form der Transfusionsreaktion dar und ist in der Regel auf eine Verwechslung der Blutgruppe zurückzuführen.
Prinzip
Antikörper des Empfängers binden an die Erythrozyten des Spenders. Dies führt zur Agglutination und in der Folge zur intravasalen Hämolyse der transfundierten Erythrozyten.
Symptome
Typische Symptome sind:
- Fieber
- Schüttelfrost
- Rückenschmerzen
- Hämoglobinurie
- Schock
Laborbefunde
Im Labor zeigen sich:
- erniedrigtes Hämoglobin
- erhöhte LDH-Werte
- erniedrigtes Haptoglobin

b) Febrile Transfusionsreaktionen
Die febrile Transfusionsreaktion ist eine vergleichsweise häufige, meist weniger schwerwiegende Reaktion.
Ursache
Sie entsteht durch Antikörper des Empfängers gegen Leukozyten oder andere Zellbestandteile im transfundierten Präparat.
Symptome
- Fieber
- Schüttelfrost

c) Allergische Transfusionsreaktion
Allergische Transfusionsreaktionen beruhen auf einer Reaktion des Immunsystems gegen Plasmaproteine des Spenders.
Symptome
- Hautausschlag
- Juckreiz
- in schweren Fällen Anaphylaxie
d) TRALI (transfusion related acute lung injury)
TRALI ist eine seltene, aber potenziell lebensbedrohliche Komplikation der Transfusion.
Ursache
Es handelt sich um eine immunologische Reaktion, die zu einer Schädigung der Lungengefäße führt.
Symptome
- akute Atemnot
- Lungenödem
e) Volumenüberladung
Eine Volumenüberladung entsteht durch die Gabe zu großer Flüssigkeitsmengen innerhalb kurzer Zeit.
Ursache
- zu schnelle oder zu umfangreiche Transfusion
Symptome
- Atemnot
- Ödeme
- Hypertonie